Récolte et clarification à l’échelle du laboratoire de vecteurs lentiviraux à l’aide des systèmes de filtration Sartoclear Dynamics Lab

Introduction
Avec l’essor des thérapies géniques et des thérapies cellulaires modifiées génétiquement, les virus sont devenus des outils essentiels en médecine. La thérapie génique présente un fort potentiel thérapeutique pour le traitement de nombreuses maladies héréditaires et acquises¹, avec trois mille essais cliniques en cours répertoriés utilisant des vecteurs viraux, dont environ 10 % impliquent des vecteurs lentiviraux². Plus de deux mille produits cellulaires modifiés génétiquement sont actuellement en développement, et quatre thérapies CAR-T ont déjà été approuvées pour des indications en oncologie. La perspective prometteuse des essais cliniques en cours sur les thérapies géniques et cellulaires³,⁴ signifie qu’il existe une forte demande en méthodes évolutives et rentables pour la production et la purification de vecteurs viraux⁵.
Les vecteurs lentiviraux (LV) sont généralement produits par transfection transitoire de cellules HEK293T avec plusieurs plasmides vecteurs⁶,⁷. Le virus est libéré dans le surnageant ; les cellules doivent donc être retirées du bouillon de culture cellulaire. L’un des défis de la recherche CAR-T réside dans l’absence d’une méthode de clarification de LV établie comme référence. Le but du processus de clarification est d’éliminer les principaux contaminants et de réduire la turbidité de la solution, tout en maintenant l’activité virale. À l’échelle du laboratoire, la clarification est habituellement réalisée par centrifugation du bouillon de fermentation, complétée par une microfiltration du surnageant¹,⁸,⁹. Simplifier la récolte et la clarification en utilisant uniquement une filtration sur membrane en une seule étape, ce qui peut être réalisé grâce à l’utilisation d’auxiliaires de filtration, améliorerait l’efficacité de la purification des LV et la transduction des cellules T.
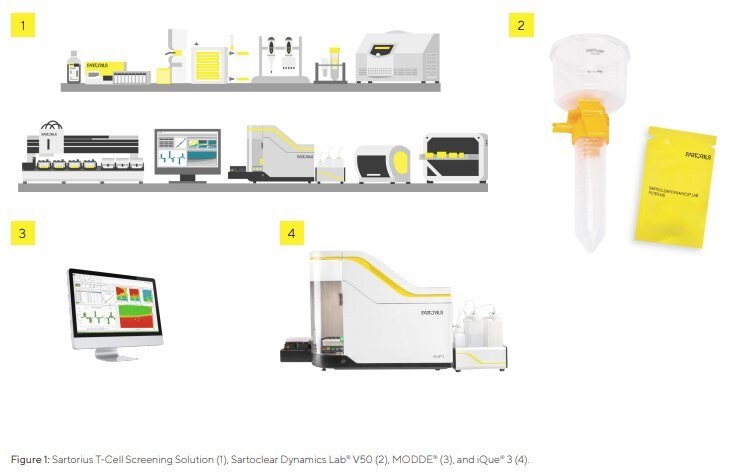
Pour simplifier les flux de travail de recherche CAR-T, la solution Sartorius T-Cell Screening propose une approche semi-automatisée et multiplexée pour la découverte de nouvelles cibles et le développement de constructions CAR efficaces (Figure 1). En particulier, la gamme de produits de filtration Sartoclear Dynamics Lab, utilisée pour clarifier les bouillons de culture cellulaire, a été développée afin de faciliter un flux de travail rapide et efficace pour la récolte de vecteurs viraux. Elle repose sur le principe de la filtration dynamique avec adjuvant filtrant. L’agent filtrant, la terre de diatomée (DE), est constitué de restes squelettiques fusionnés de diatomées présentant une structure hautement poreuse¹⁰. Après le procédé amont, le bouillon de culture est d’abord mélangé à l’agent filtrant, puis appliqué sur une membrane de filtration. La DE forme un gâteau poreux quasi incompressible, et sa grande porosité permet au liquide de circuler autour des particules, empêchant l’encrassement du filtre¹¹. L’utilisation d’auxiliaires de filtration élimine l’étape de centrifugation et réduit le temps de traitement.
Matériel et méthodes
Le vecteur lentiviral a été exprimé par transfection transitoire de cellules HEK293T/17 SF cultivées en suspension dans le bioréacteur à usage unique UniVessel 2 L (Sartorius), avec quatre plasmides codant les gènes lentiviraux essentiels, tel que décrit en détail par Labisch et al.¹²
La clarification de 50 mL d’échantillons de bouillon de culture LV a été réalisée en utilisant la version polyéthersulfone (PES) 0,45 μm du Sartoclear Dynamics Lab V50 (Sartorius). Le kit Sartoclear Dynamics Lab V50 contient des unités de filtration sous vide Sartolab RF50, composées d’un entonnoir, d’un tube conique de 50 mL et d’un connecteur pour raccordement au vide. Le kit est fourni avec un choix de quantités standard de 1 g de DE (Sartorius, SDLV-0050-01F0-2) ou 2 g de DE (Sartorius, SDLV-0050-02F0-2) pour la filtration de volumes allant jusqu’à 50 mL. Des concentrations de DE comprises entre 5 g/L et 40 g/L de bouillon de culture ont été testées. La DE a été ajoutée à 50 mL de bouillon, mélangée pour obtenir une suspension homogène, puis immédiatement filtrée. De plus, la clarification de 50 mL de bouillon a été réalisée sans DE selon une méthode en deux étapes : centrifugation pendant 5 min à 800 × g, suivie d’une filtration à travers un Sartolab RF50 avec membrane PES de 0,45 μm (Sartorius, 180F01---------2). Pour déterminer la capacité du filtre, la clarification a été poursuivie jusqu’à colmatage du filtre, et le volume de filtrat obtenu a été mesuré. La filtration sous vide a été effectuée avec le Sartolab MultiStation (Sartorius, SDLC01), un support conçu pour accueillir une à six unités Sartolab RF50, permettant la filtration simultanée jusqu’à six échantillons.
Une approche de conception d’expériences (DOE) a été utilisée pour optimiser les conditions de clarification. La concentration de DE a été variée entre 5 g/L, 12,5 g/L et 20 g/L, et le temps de contact entre 0, 10 et 20 minutes. Les expériences ont été planifiées comme un plan factoriel complet avec quatre points centraux et évaluées à l’aide du logiciel MODDE™ (Sartorius). Les paramètres analytiques utilisés pour évaluer les performances de clarification étaient les suivants: mesure de la turbidité à l’aide du turbidimètre Orion™ AQUAfast AQ3010 (Thermo Fisher Scientific) ; concentration totale d’ADN double brin (Quant-iT™ PicoGreen™, Thermo Fisher Scientific) ; et concentration totale de protéines (kit d’essai protéique Pierce™ Coomassie Bradford, Thermo Fisher Scientific), avant (matériel centrifugé) et après la filtration. En outre, le titre en particules de LV a été déterminé par ELISA p24 (QuickTiter™ Lentivirus Titer Kit, Cell Biolabs). Le titre en particules lentivirales infectieuses a été mesuré par transduction de cellules HEK293T adhérentes avec les échantillons viraux et mesure de l’expression du transgène (construct CAR-CD19) par cytométrie en flux avec l’iQue Screener PLUS (Sartorius), comme décrit précédemment¹².
Résultats et discussion
Évaluation de l’impact de la concentration de DE et du temps de contact avec la DE sur la turbidité, le titre infectieux et le temps de filtration dans une étude DOE utilisant MODDE
Pour étudier l’effet de la DE sur la clarification des LV, les facteurs concentration de DE et temps de contact ont été sélectionnés dans une approche DOE afin d’évaluer leur influence sur la turbidité, le titre infectieux et le temps de filtration. La densité cellulaire totale du bouillon utilisé dans les essais de filtration du DOE était de 3,7 × 10⁶ cellules/ml, avec une turbidité de 382 NTU.
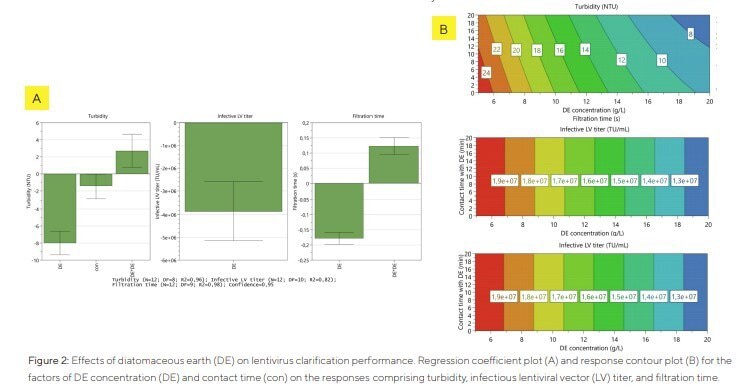
La Figure 2 montre que les réponses concernant le titre infectieux et le temps de filtration ne sont influencées que par la concentration de DE. À mesure que la concentration de DE augmente, le titre infectieux diminue linéairement. Pour le temps de filtration, un terme quadratique apparaît, entraînant une réduction du temps de filtration à mesure que la concentration de DE augmente dans la plage testée. La turbidité a été réduite linéairement à mesure que le temps de contact avec la DE augmentait. De plus, l’augmentation de la concentration de DE a diminué la turbidité, ce facteur ayant l’effet le plus prononcé.
Évaluation de l’impact du Sartoclear Dynamics Lab V50 sur le temps de traitement
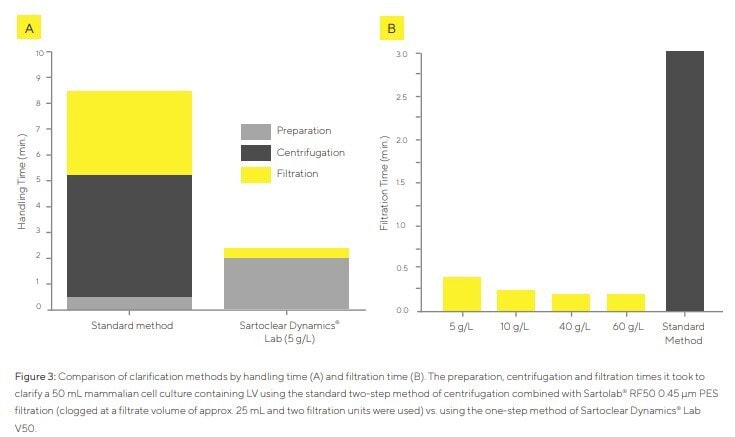
La manipulation du kit Sartoclear Dynamics Lab V50 avec différentes concentrations de DE a été comparée à la microfiltration du surnageant centrifugé utilisant Sartolab RF50 (méthode standard en deux étapes). Après la récolte, la densité cellulaire était de 1,11 × 10⁶ cellules/ml et la turbidité de 141 NTU. Le temps de traitement total a été réparti en temps de préparation (mesure des volumes, retrait du surnageant, pesée et ajout de DE), temps de centrifugation et temps de filtration.
Lors de la clarification du surnageant centrifugé, le premier filtre Sartolab RF50 s’est colmaté après environ 25 mL, nécessitant l’utilisation d’un second filtre, ce qui a rendu la procédure plus laborieuse. L’utilisation de Sartoclear Dynamics Lab V50 a réduit le temps de préparation en éliminant la centrifugation (Figure 3A). Le temps de manipulation a été réduit d’un facteur 3,8 par rapport à la méthode standard. Le temps de filtration dépendait de la concentration de DE : 25 s à 5 g/L et jusqu’à 13 s à 60 g/L (Figure 3B).
Évaluation de l’impact du Sartoclear Dynamics Lab V50 sur la turbidité et la capacité de filtration
La clarification a été effectuée avec Sartoclear Dynamics Lab V50 à 5 g/L de DE ou avec la méthode conventionnelle en deux étapes. Le bouillon contenant les lentivirus utilisé pour la mesure de capacité avait une densité cellulaire totale de 3,7 × 10⁶ cellules/ml et une turbidité de 398 NTU au moment de la récolte.
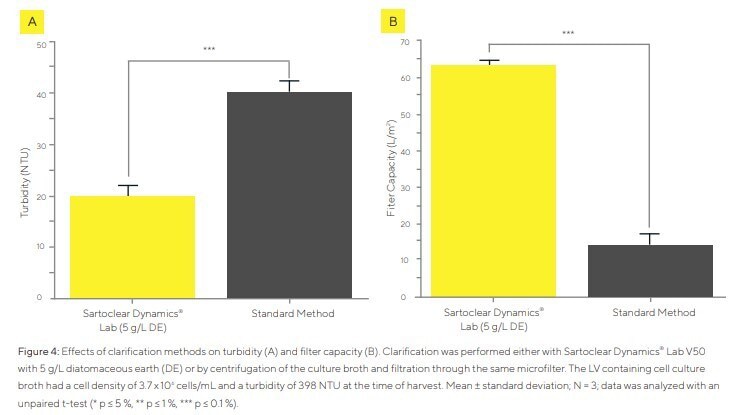
Selon la Figure 4A, la méthode conventionnelle donne une turbidité de 43 NTU (réduction de 89 %), tandis que Sartoclear Dynamics Lab V50 la réduit de 95 %, à 21 NTU. Les capacités de filtration ont été déterminées avec 5 g/L de DE. La filtration s’est poursuivie jusqu’au colmatage. Le procédé conventionnel entraîna un colmatage rapide après 33 mL. Avec 5 g/L de DE, le volume filtrable dépassa plus de deux fois la capacité nominale de 50 mL. Les capacités de filtration augmentèrent fortement (Figure 4B). Le procédé classique donna 15 L/m², tandis que 5 g/L de DE permirent d’atteindre environ 63 L/m². Après clarification avec DE, le titre infectieux de LV était généralement ≥ 75 % par rapport au matériel centrifugé.
Évaluation de l’impact du Sartoclear Dynamics Lab V50 sur l’élimination des impuretés
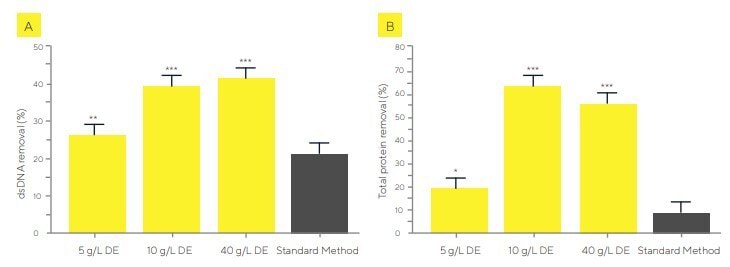
Dans une expérience distincte, le potentiel du Sartoclear Dynamics Lab V50 pour éliminer les impuretés liées au procédé a été analysé en quantifiant l’élimination totale des protéines et de l’ADN double brin (dsDNA) (Figure 5).
Une concentration de DE allant jusqu’à 10 g/L a augmenté l’élimination des protéines et du dsDNA, mais des concentrations plus élevées, entre 10 g/L et 40 g/L, n’ont entraîné aucune amélioration supplémentaire. En revanche, l’utilisation du Sartoclear Dynamics Lab V50 a permis une élimination significativement plus élevée des impuretés que la méthode standard en deux étapes de centrifugation et de filtration.
Conclusion
Les systèmes de filtration Sartoclear Dynamics Lab permettent la clarification de cultures cellulaires de mammifères contenant des LV sans nécessiter de centrifugation. Par rapport à la méthode standard, le Sartoclear Dynamics Lab V50 a montré une meilleure réduction de la turbidité, une élimination supérieure des contaminants et une capacité membranaire plus élevée. Cela confirme l’adéquation des systèmes de filtration Sartoclear Dynamics™ Lab pour la récolte et la clarification des vecteurs lentiviraux. Il est toutefois nécessaire d’ajuster la concentration de DE afin de récupérer des rendements élevés de LV et d’éviter des pertes dues à une quantité de DE excessivement élevée. Le kit Sartoclear Dynamics Lab V50 avec DE permet au technicien de laboratoire d’effectuer une filtration clarifiante en une seule étape, facilitant non seulement une manipulation plus rapide et plus sûre, mais réduisant également la quantité de consommables utilisés. Le kit permet de sélectionner une quantité optimisée de DE, augmentant considérablement la capacité du filtre et garantissant ainsi un processus de clarification de lentivirus efficace et robuste en thérapie génique et en thérapie cellulaire modifiée.
Références
1 Segura, M. M., Kamen, A. A., and Garnier, A. 2011. Overview of current scalable methods for purification of viral vectors. Methods Mol Biol 737, 89–116.
2 John Wiley & Sons, Inc. 2019. Gene therapy trials worldwide. John Wiley & Sons, Inc, Hoboken, NJ, USA. J Mark Access Health Policy. Accessed 5 May 2020.
3 Hanna, E., Rémuzat, C., Auquier, P., et al. 2017. Gene therapies development: slow progress and promising prospect. Journal of market access & health policy 5, 1, 1265293.
4 Herzog, R. W., Cao, O., and Srivastava, A. 2010. Two decades of clinical gene therapy--success is finally mounting. Discov Med 9, 45, 105–111.
5 Ruscic, J., Perry, C., Mukhopadhyay, T., et al. 2019. Lentiviral Vector Purification Using Nanofiber Ion-Exchange Chromatography. Molecular therapy. Mol Ther Methods Clin Dev 15, 52–62.
6 Merten, O.-W., Schweizer, M., Chahal, P., et al. 2014. Manufacturing of viral vectors: part II. Downstream processing and safety aspects. Pharmaceutical Bioprocessing 2, 3, 237–251.
7 Sakuma, T., Barry, M. A., and Ikeda, Y. 2012. Lentiviral vectors: basic to translational. Biochem J 443, 3, 603–618.
8 Bauler, M., Roberts, J. K., Wu, C.-C., et al. 2020. Production of Lentiviral Vectors Using Suspension Cells Grown in Serum-free Media. Mol Ther Methods Clin Dev 17, 58–68.
9 Rodrigues, T., Carrondo, M. J. T., Alves, P. M., et al. 2007. Purification of retroviral vectors for clinical application: biological implications and technological challenges. J Biotechnol 127, 3, 520–541.
10 Bakr, H. E. G. M. 2010. Diatomite: Its Characterization, Modifications and Applications. Asian J Mater Sci 2, 3, 121–136.
11 Grauf, M., Lagrange, B., and Schöne, K. 2018. Simplified Small-Scale Harvest of CHO Cells for mAb Analytics. Genetic Engineering & Biotechnology News 38, 5, 22– 23.
12 Labisch, J. J., Bollmann, F., Wolff, M. W., et al. 2021. A new simplified clarification approach for lentiviral vectors using diatomaceous earth improves throughput and safe handling. J Biotechnol, 326, 11–20.
Abréviations
CAR - Récepteur d’antigène chimérique
(ds)DNA - ADN (double brin) désoxyribonucléique
DE - Terre de diatomées
DOE - Plan d’expériences
HEK - Cellules rénales embryonnaires humaines
LV - Vecteur lentiviral
PES - Polyéthersulfone
TU - Unités de transduction
VP - Particules virales